放射線利用技術データベースのメインページへ
作成: 1999/12/10 日下部 俊男
データ番号 :040202
加速器質量分析法を用いたアルミニウム代謝の研究
目的 :加速器質量分析法を用いた生体中のアルミニウム代謝の研究と筋萎縮性側索硬化症やアルツハイマー病の発症機構の解明
放射線の種別 :軽イオン,重イオン
放射線源 :タンデムバンデグラフ加速器(20MV),Middleton型セシウムスパッタ負イオン源(AlO-,100nA),タンデム型静電加速器(5MV),セシウムスパッタ負イオン源,他
利用施設名 :ペンシルバニア大学加速器質量分析施設,ダレスバリィー研究所核構造施設,東京大学原子力総合センタータンデム静電加速器
照射条件 :真空中
応用分野 :医学,生物科学
概要 :
筋萎縮性側索硬化症やアルツハイマー病の病因解明のため,生体中のアルミニウム代謝の研究手段の一つとして,26Alをトレーサーとする実験方法が,加速器質量分析法(AMS)で確立してきた。AMSでは,極微量のAlしか必要とせず,低被曝線量下での生体(ラットや人体など)における実験が可能となった。ラットの腹腔内に26Alを注射すると,数日後には脳内に容易に進入し,しかも長期間残存することもわかった。
詳細説明 :
筋萎縮性側索硬化症やアルツハイマー病の発症の要因として種々の説が検討されてきたが,脳や脊髄などの神経繊維にアルミニウムが高濃度に沈着するアルミニウム代謝異常説が有力になりつつある。これまでの初期の研究では,脊髄や大脳組織に蓄積されたアルミニウムなどの微量元素を死後,種々の分析法を駆使して測定するものであり,アルミニウムの蓄積の過程そのものが病因なのかあるいは発病の結果としてそれが蓄積されるのかがはっきりしなかった。これは一方で,アルミニウムが地表面上でありふれた元素の一つであり,飲食物から日常的に摂取しており,脳-血液関門作用で容易にはアルミニウムが脳内などの神経組織に取り込まれないという「常識」があったためでもある。
そこで,アルミニウムを生体トレーサーとして,その脳などへの蓄積過程の研究が必要となってきた。ところが,アルミニウムの同位体は,安定な27Alの他に,24Al,25Al,26Al,26mAl,28Al,29Al,30Alがあるが,これらの半減期はそれぞれ,2.14秒,7.24秒,7.2×105年,6.36秒,2.31分,6.6分,3.3秒と,日,週,月,年のオーダーの生体的変化を研究するには,26Al以外は半減期が短すぎ,トレーサーとしての研究は困難である。26Alも逆に半減期が長すぎ,多量の26Alが必要となるため,従来の放射線計測法ではこれも用いることが事実上困難であった。しかし加速器質量分析法(AMS)の開発により,微量な26Alトレーサーを用いた実験が可能となった。
Meiravらは,0.35ngの26Alと40ngの27Alを含んだ塩水を静脈注射し,その後5時間後から3週間にわたって血清と尿を採取した。26Al/27Al比が10-10から10-14と10%以下の誤差で測定された。

図1 The data shown is the fraction of the administered 26Al remaining in the blood and excreted in the urine as a function of time after injection as measured in the present experiment. The horizontal bars indicate the duration of the urine collection. The curves are the results of a three-compartment simulation using the clearance values given in the text. (原論文1より引用。 Reproduced from Nucl. Instr. Meth. Phys. Res., vol.B52, 536 (1990), O.Meirav, R.A.L.Sutton, D.Fink, R.Middleton, J.Klein, V.R.Walker, A.Halabe, D.Vetterli, R.R.Johnson: Application of accelerator mass spectrometry in aluminum metabolism studies, Figure 2 (Data source 1, pp.538), Copyright (1990), with permission from Elsevier Science.)
図1に示すように,ラットの血および尿中の26Al残存量は,最初の1日間で指数関数的に急激に減少し,そこから先は緩やかに減少している。この減少過程を彼らは図2に示すような「3成分」モデルで説明している。
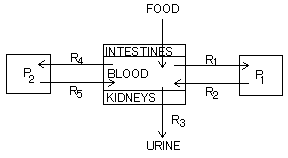
図2 Box diagram of the three-compartment aluminium model that was used to simulate the experiment. The Ri's are the fractional clearance coefficients. (原論文1より引用。 Reproduced from Nucl. Instr. Meth. Phys. Res., vol.B52, 536 (1990), O.Meirav, R.A.L.Sutton, D.Fink, R.Middleton, J.Klein, V.R.Walker, A.Halabe, D.Vetterli, R.R.Johnson: Application of accelerator mass spectrometry in aluminum metabolism studies, Figure 3 (Data source 1, pp.538), Copyright (1990), with permission from Elsevier Science.)
さらに彼らは,投与する26Alの放射能は約30pCiと見積もられ,自然界のバックグラウンドからの被曝量の0.1%以下であるので人体にも適用可能であるとしている(AMSによる26Alトレーサーの人体へ応用は,LitherlandやElmoreが提案した)。
Barkerらは,ダレスバリー研究所の20MVタンデムバンデグラーフ加速器を用いたAMS法で,人体におけるアルミニウム吸収実験を確立した。100ngの26Alを含んだ溶液を経口で人体に与え,6,12,18時間後の血液中に移行したアルミニウムの形態を調べた。また,574Bqの26Al溶液を人体に静脈注射し,その後106日間に渡って血中の26Al残存量を測定し,Meiravらのラットに対するのと良く似た時間依存性を得た。
湯本や小林らは,東京大学原子力総合センターのタンデム加速器を使用し,ラットの腹腔内に10dpm(2.35×10-10g)の26Alと2.75mgの27Alとの混合溶液を注射し,血液だけでなく肝臓と脳についても,26Al残存量の経時変化を測定した。彼らは1990年に,注射後5から35日間に渡る測定結果を一旦報告しているが,その後270日に渡る測定結果を1997年に報告している。
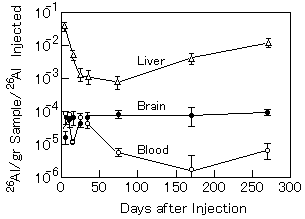
図3 Time course of 26Al levels in the liver, blood and brain (cerebrum) after a single 26Al injection. The 26Al level in the brain did not decrease over 270 days after injection. On the contrary, the blood 26Al level decreased remarkably 75 days after injection. (原論文4より引用。 Reprinted from Nucl. Instr. Meth. Phys. Res., S.Yumoto, H.Nagai, M.Imamura, H.Matsuzaki, K.Hayashi, A.Masuda, H.Kumazawa, H.Ohashi, K.Kobayashi: 26Al uptake and accumulation in the rat brain, Figure 1 (Data source 4, pp.280), Copyright (1997), with permission from Elsevier Science.)
図3に示すように,注射された26Alの大部分は肝臓内で観測され,その中の残存量は始め急激に減少し,25日目で5日目の約50分の1となっている。その後25日から75日の間はほぼ一定で,それ以降はむしろ単調に増大している。注射後5日目の最初の測定で既に,血中や脳内にもほぼ同じ量の26Alが検出されている。血液中の26Al残存量は,約35日目までほぼ一定だがその後10分の1位に減少するのに対し,脳内のそれは270日までほぼ一定に保たれている。
この結果,アルミニウムに対しては脳-血液関門があまり作用せず,比較的短期間に脳内に取り込まれ,かつ一旦脳内に取り込まれたアルミニウムは長期間残存し続けることが分かった。
コメント :
確かに26Alトレーサーを用いた生体実験では,他の方法では事実上困難であり,AMSが唯一有力な手段と言えるであろう。しかし筋萎縮性側索硬化症やアルツハイマー病の病因解明の観点から言えば,アルミニウムは地表面上で普遍的な元素の一つであり,神経組織へのアルミニウム沈着機構における他の元素との協調関係を調べる必要があると思われる(近畿大・水本良彦[故人]説)。
原論文1 Data source 1:
Application of accelerator mass spectrometry in aluminum metabolism studies
O.Meirav, R.A.L.Sutton, D.Fink, R.Middleton, J.Klein, V.R.Walker, A.Halabe, D.Vetterli and R.R.Johnson
Department of Physics and Department of Medicine, University of British Columbia, Vancouver, BC, Canada V6T 1W5. Department of Physics, University of Pennsylvania, Philadelphia, Pennsylvania 19104, USA
Nuclear Instruments and Methods in Physical Research, B52 (1990) 536-539
原論文2 Data source 2:
Development of 26Al accelerator mass spectrometry for aluminium absorption experiments in humans
J.Barker, J.P.Day, N.D.Priest, D.Newton, P.V.Drumm, J.S.Lilley and G.W.A.Newton
Department of Chemistry, University of Manchester, Manchester M13 9PL, UK. Biomedical Research Department, AEA Environment and Energy, Harwell Laboratory, Oxfordshire OX11 0RA, UK. Nuclear Structure Facility, SERC Laboratory, Daresbury, Warrington WA4 4AD, UK
Nuclear Instruments and Methods in Physical Research, B68 (1992) 319-322
原論文3 Data source 3:
26Al Tracer Experiment by Accelertor Mass Spectrometry and its Application to the Studies for Amyotrophic Lateral Sclerosis and Alzheimer's Disease. I.
K.Kobayashi*), S.Yumoto2*), H.Nagai3*), Y.Hosoyama3*), M.Imamura4*), S.Masuzawa3*), Y.Koizumi5*), and H.Yamashita6*)
*)Research Center for Nuclear Science and Technology, University of Tokyo, Yayoi 2-11-16, Bunkyo-ku, Tokyo 113, Japan. 2*)Department of Anatomy, Faculty of Medicine, University of Tokyo, Hongo 7-3-1, Bunkyo-ku, Tokyo 113, Japan. 3*) College of Humanities and Sciences, Nihon University, Sakurajousui 3-25-40, Setagaya-ku, Tokyo 156, Japan. 4*)Institute for Nuclear Study, University of Tokyo, Tanashi, Tokyo 188, Japan. 5*)Radioisotope Center, University of Tokyo, Yayoi 2-11-16, Bunkyo-ku, Tokyo 113, Japan. 6*)Department of Physics, Faculty of Science, University of Tokyo, Bunkyo-ku, Hongo 7-3-1, Tokyo 113, Japan.
Proc. Japan Acad., Vol. 66, Ser. B, No. 10 (1990) 189-192
原論文4 Data source 4:
26Al uptake and accumulation in the rat brain
S.Yumoto*)2*), H.Nagai3*), M.Imamura4*), H.Matsuzaki5*), K.Hayashi3*), A.Masuda3*), H.Kumazawa3*), H.Ohashi6*), K.Kobayashi7*)
:)Department of Anatomy, Faculty of Medicine, University of Tokyo, Hongo 7-3-1, Bunkyo-ku, Tokyo 113, Japan. 2*)Yumoto Institute of Neurology, Kawadacho 6-11, Shinjuku-ku, Tokyo 162, Japan. 3*)College of Humanities and Sciences, Nihon University, Japan. 4*)Institute for Nuclear Study, University of Tokyo, Tokyo, Japan. 5*)Institute for Cosmic Ray Research, University of Tokyo, Tokyo, Japan. 6*) Laboratory of Physics, Tokyo University of Fisheries, Tokyo, Japan. 7*) Research Center for Nuclear Science and Technology, University of Tokyo, Tokyo, Japan
Nuclear Instruments and Methods in Physical Research, B123 (1997) 279-282
参考資料1 Reference 1:
加速器質量分析法による極微量放射性同位体測定 -生物科学・医学試料への応用-
中村俊夫
名古屋大学年代測定試料研究センター(〒464-01 名古屋市千種区不老町)
蛋白質 核酸 酵素, Vol. 39 No. 11 (1994) 2011-2020
参考資料2 Reference 2:
筋萎縮性側索硬化症頸髄における微量元素のα線励起蛍光X線分析
水本 良彦,岩田 志郎,笹島 和久,八瀬 善郎,吉田 宗平
近畿大学理工学部原子炉工学科 577 東大阪市小若江3丁目4-1. 京都大学原子炉実験所ホットラボ設備部門 590-04 大阪府泉南郡熊取町野田. 和歌山県立医科大学神経病研究部 640 和歌山市9番丁9
Radioisotopes, Vol. 29, No. 12 (1980) 585-589
参考資料3 Reference 3:
中性子放射化分析法および蛍光X線分析法による筋萎縮性側索硬化症脊髄のCa/P原子比の測定
水本 良彦,岩田 志郎,笹島 和久,吉田 宗平,吉益 文夫,八瀬 善郎
近畿大学理工学部原子炉工学科 577 東大阪市小若江3-4-1. 京都大学原子炉実験所ホットラボ設備部門 590-04 大阪府泉南郡熊取町野田. 和歌山県立医科大学神経病研究部 640 和歌山市9番丁9
Radioisotopes, Vol. 32, No. 11, (1983) 551-554
参考資料4 Reference 4:
Ultrasensitive Radioisotopes, Stable-Isotope, and Trace-Element Analysis in the Biological Sciences Using Tandem Accelerator Mass Spectrometry
D.Elmore
Nuclear Structure Research Laboratory, University of Rochester, Rochester, NY 14627
Biological Trace Element Research, Vol. 12, (1987) 231-245
キーワード:加速器質量分析法、筋萎縮性側索硬化症、アルツハイマー病、26Alトレーサー、アルミニウム毒性、アルミニウム代謝、アルミニウム蓄積
accelerator mass spectrometry, amyotrophic lateral sclerosis, Alzheimer's disease, 26Al tracer, aluminum toxicity, aluminum metabolism, aluminum accumulation
分類コード:040101, 040405, 030404
放射線利用技術データベースのメインページへ

