放射線利用技術データベースのメインページへ
作成: 2002/01/13 鷲野 弘明
データ番号 :030227
PET用腫瘍診断剤:F-18-フルオロコリン、F-18-フルオロアミノ酸
目的 :18F-フルオロコリン、18F-フルオロアミノ酸に関する研究動向の紹介
放射線の種別 :陽電子
利用施設名 :PET使用施設
応用分野 :医学、診断
概要 :
18F-フルオロコリンや18F-フルオロアミノ酸は、近年注目されるPET用診断剤であり、CTやMRIでは診断しにくい腫瘍への適用が研究されている。18F-フルオロコリンは、腫瘍細胞で亢進しているコリン代謝を反映して腫瘍細胞内に取り込まれ、脳腫瘍・前立腺癌・乳癌などの診断に有用である。18F-フルオロアミノ酸は、天然アミノ酸ではないため蛋白質に取り込まれないが、アミノ酸代謝速度に応じて細胞内に集積すると考えられ、脳腫瘍などの診断に有用である。これらは、特に18F-FDGが適用できない腫瘍への利用を目指して研究されており、今後の進展が期待される。
詳細説明 :
腫瘍の画像診断は、通常CTやMRIで行われる。しかし、良性/悪性の鑑別・手術後再発部位の診断・他病変との鑑別などは、たとえ造影剤を用いてもCT・MRIでは難しいケースがある。そのようなとき、CT・MRIを補助する画像診断として、18F-2-fluoro-2-deoxyglucose(18F-FDG)によるPET診断が利用されている。しかし、18F-FDGは、診断メカニズム上ブドウ糖代謝の盛んな正常組織(例えば脳)や急性期の炎症組織に集積するため、脳腫瘍や治療直後の診断などには使用しにくい。それ故、18F-FDGを補完するPET用腫瘍診断剤の研究開発が、近年盛んになっている。
近年注目されている研究途上のPET用腫瘍診断剤として、18F標識チミジン誘導体、18F標識アミノ酸誘導体、18F標識コリン誘導体がある。これらは、それぞれ盛んな細胞増殖に伴って亢進するDNA合成、蛋白質合成、またはコリンの利用に着目した診断剤であり、悪性腫瘍の盛んな細胞増殖を画像化するものである。ここでは、18F-フルオロコリン誘導体の代表例として18F-fluoromethyl-dimethyl-2-hydroxyethylammonium (18F-FCH)、及び18F-フルオロアミノ酸誘導体の代表例として18F-1-amino-3-fluorobutane-1-carboxylic acid (18F-FACBC)を紹介する。これらのトレーサーは、いずれもまだ研究段階にあり、我が国においてはまだ日常診療には使用されていない。
18Fは、サイクロトロンで生産される物理的半減期110分の放射性核種であり、ポジトロン(β+)を放出する。β+は、極めて半減期の短い粒子で消滅の際に510keVのγ線を2本反対方向に放射する。この2本のγ線放射を同時に捕らえて画像化する装置がポジトロンエミッションCT(PET)である。PETは、核医学画像診断装置の中では定量性や空間分解能に優れる。
1. 18F-フルオロコリン誘導体 - 18F-FCH
RI標識コリン誘導体が腫瘍イメージング剤になり得ることに初めて着目し報告したのは、Haraら日本人研究者である。彼らは、最初11C標識コリンで研究を開始し、さらに実用性の高い18F-フルオロコリン誘導体へと進み、この領域の研究を切り開いた。
コリンの腫瘍組織における動態は、多くのMR spectroscopyや生化学的研究から明らかになりつつある。即ち、活発な細胞分裂を繰り返す腫瘍細胞では、コリンキナーゼ活性が亢進し、choline, phosphocholine, phosphoethanolamineの細胞内濃度が上昇している。これは、細胞膜リン脂質の合成の亢進と符合する。コリン代謝の亢進は、脳腫瘍・前立腺がん・乳がんなどで確認されている。RI標識コリン誘導体の例を図1に示す。
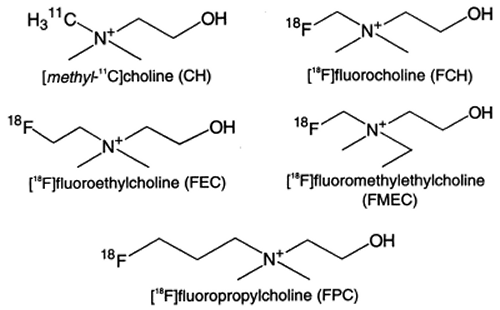
図1 18F標識フルオロコリン誘導体の化学構造。
コリンは細胞内に取り込まれた後、コリンキナーゼによってリン酸化され、マイナスの電荷が付与される。このマイナス電荷は、18F-FDGの場合と同様にRI標識コリンの細胞外への透過拡散を阻止すると思われ、これによってRI標識コリンが腫瘍組織に高濃度に集積すると推察される。In vitro細胞実験の結果では、図1のFCHはコリンとほぼ同程度にリン酸化されるが、FECとFPCはコリンの各々30%及び60%程度である。
11C標識コリンは、投与後に極めて速やかに血液中より消失し、肝臓に集積し腹腔内には滞留するものの脳・肺・心臓・筋肉・骨などには集積しないため、腹部以外の部位、即ち頭頚部・胸部・四肢では優れたコントラストが得られる。
以下図2に18F-フルオロコリン誘導体(18F-FCH)を前立腺がん患者に投与した結果を紹介する。上段の図Aは投与2〜4分における骨盤部のPET画像(縦断像)である。前立腺部位に相当する異常集積が見られる。18F-FCHの血中消失は極めて速く、投与後2分以内にピークレベルの5%以下にまで落ちる。そのため、投与直後より放射能が血液から消失し腎臓を経て膀胱内に届くまで間、骨盤腔を観察することができる。この4分間の様子は、中段図Bの時間-放射能曲線が示しており、2〜4分の2分間が絶好の観察時間帯である。この患者の全身像は、図Cに示した。この画像より、縦隔領域に異常集積が認められ、この部位のリンパ節への転移が疑われた。
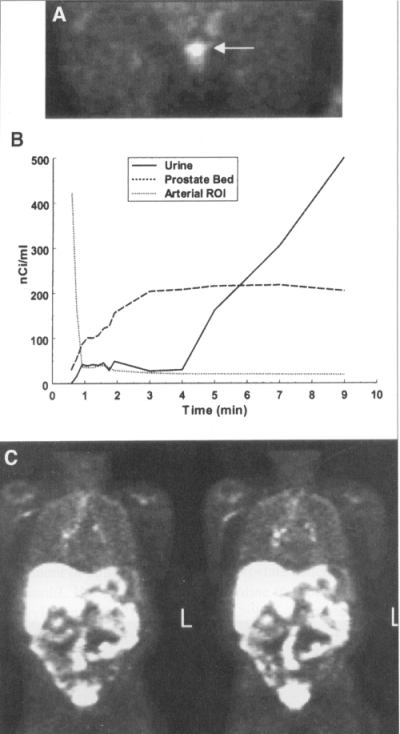
図2 前立腺がん患者における18F-FCHイメージング。 A:投与2〜4分後における骨盤腔のイメージ。前立腺の部位に一致して異常集積が認められる。 B:図Aにおける各領域の時間-放射能曲線。膀胱(Urine)、前立腺(Prostate Bed)、腸骨動脈(Arterial ROI) C:体幹部のイメージ。
以下図3に乳癌患者を対象に18F-FCHイメージングと18F-FDGイメージングを行った例を示す。上段の18F-FDGでは、心臓への集積が見られ、下段の18F-FCHでは唾液腺・肝臓・腎臓などへの集積が見られる。これらは、いずれも各トレーサー特有の正常臓器への分布である。FCH及びFDGは、ともに胸骨への大きな転移、右肺門及び気管傍リンパ節への転移、右前方の骨盤への転移を示している。しかし、リンパ節転移の描出能力はFCHの方が高い。
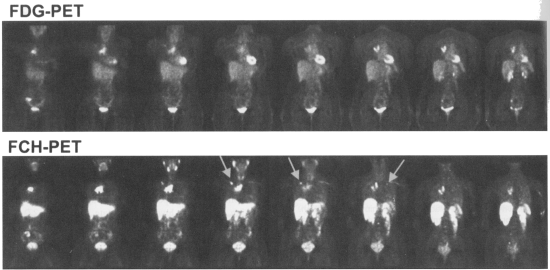
図3 乳がん患者における18F-FCHイメージと18F-FDGイメージの比較。上段:18F-FDG、下段:18F-FCH。
2. 18F標識アミノ酸誘導体 - 18F-FACBC
ここ20数年来、様々な標識アミノ酸が腫瘍イメージング剤として研究されてきた。中でもメチオニン、フェニルアラニン、チロシン、トリプトファンなどの天然アミノ酸は、SPECT核種であるI-123やPET核種であるC-11、F-18などで標識され、良い結果が得られている。これとは別に、生体内で利用されない非天然型アミノ酸の腫瘍への集積も研究されてきた。これらの非天然型アミノ酸は、蛋白質に取り込まれることはないが、アミノ酸トランスポート系により細胞内に輸送されれば、アミノ酸代謝の過程を画像化しうると期待されている。
今まで報告された非天然型アミノ酸のうち選択性の高い化合物は、α-aminocyclobutane carboxylic acid(ACBC)、α-aminocyclopetane carboxylic acid(ACPC) α-aminoisobutyric acid(AIB)などである。Washburnらは、このうち11C-ACBCが最も選択的に取り込まれることを動物実験で示した。この化合物を用いて星状細胞腫患者を対象に行った臨床試験でも、高い腫瘍取り込みと低いバックグラウンド(=正常脳組織への低い集積)が観察された。これらの知見をもとに、より半減期が長く使いやすいF-18化合物の研究がGoodmanらによって行われ、有望な結果が得られている。以下に18F-F ACBCの化学構造を示す。
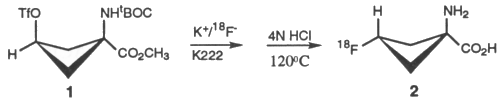
図4 18F-FACBCの標識反応及び化学構造(2)。
FACBCが、どのように血液脳関門を通過し細胞内へ輸送されるのか、まだ完全に明らかにはなっていない。FACBCの細胞内への集積程度は、非天然型中性アミノ酸の中では、Na依存性アラニントランスポート系(A-system)を経て取り込まれるAIBと、Na非依存性平衡ロイシントランスポート系(L-system)を経て取り込まれるcycloleucineの中間に位置する。FACBCは、これらアミノ酸トランスポート系により細胞内に取り込まれるものと推測される。
以下に、神経膠芽腫患者を対象に行った試験結果を示す。この例は、Gd造影MRIでは神経膠芽腫の広がりを正しく診断できず、腫瘍の切除が失敗に終わった例である。この患者は、上段のGd造影MRI/T1強調画像(頭部横断像)で左前頭葉に腫瘍が広がっていることが分かる。脳腫瘍の位置を確認して手術を行ったが、手術1週間後に実施した18F-FACBCイメージング(下段)で、はっきりとした異常集積を認めた。手術8週間後に実施した18F-FDGイメージング(中段)では、18F-FDGが正常脳組織に集積するため、腫瘍の存在は明瞭に指摘できない。下段の異常集積部分は、再手術により神経膠芽腫の遺残と確認された。
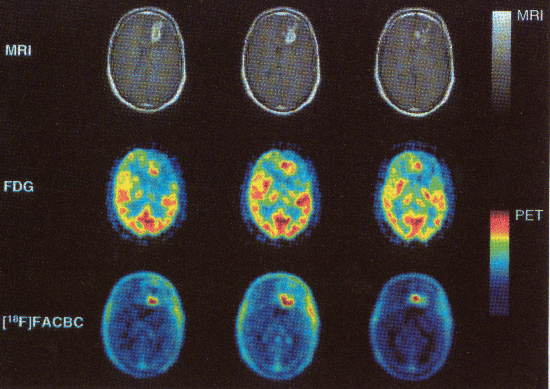
図5 神経膠芽腫患者における18F-FACBCイメージング。
上段:手術前のGd造影T1強調MRI頭部横断像。中段:手術8週間後の18F-FDG像。下段:手術1週間後の18F-FACBC像。
これらの実験例から明らかなとおり、フルオロコリンやフルオロアミノ酸は、従来の診断剤では困難な腫瘍診断において有用性が期待されている。
原論文1 Data source 1:
Synthesis and evaluation of 18F-labeled choline analogs as oncologic PET tracers.
T.R. DeGrado, S.W. Baldwin, S. Wang, M.D. Orr et al.
J. Nucl. Med. 42, p.1805-1814, 2001
原論文2 Data source 2:
Synthesis and evaluation of [18F]1-amino-3-fluorocyclobutane-1-carboxylic acid to image brain tumors. T.M. Shoup, J. Olson, J.M. Hoffman, J. Votaw et al.
J. Nucl. Med. 40, p.331-338, 1999
参考資料1 Reference 1:
Analysis of cytosolic phosphoethanolamine and ethanolamine and their correlation with prognostic factors in breast cancer.
T. Kano-Sueoka, T. Watanabe, T. Miya & H. Kasai.
Jpn J. Cancer Res. 82, p.829-834, 1991.
参考資料2 Reference 2:
PET imaging of brain tumor with [methyl-11C]choline.
T. Hara, N. Kosaka, N. Shinoura & T. Kondo.
J. Nucl. Med. 38, p.842-847, 1997.
参考資料3 Reference 3:
.Automated synthesis of fluorine-18 labeled choline analogue: 2-fluoroethyl-dimethyl-2-oxyethylammnonium [abstract].
T. Hara, M. Yuasa, & H. Yoshida.
J. Nucl. Med. 38(suppl), p.44, 1997.
参考資料4 Reference 4:
Effect of structure on tumor specificity of alicyclic α-amino acids.
L.C. Washburn, T.T. Sun, J.B. Anon & R. Hayes.
Cancer Res. 38, p.2271-2273, 1978.
参考資料5 Reference 5:
Carbon-11-methionine and PET an effective method to image head and neck cancer.
S. Leskin-Kallio, K. Nagren, P. Lehikoinen, U. Ruotsalainen et al.
J. Nucl. Med. 33, p.691-695, 1992.
キーワード:画像診断, ポジトロンエミッショントモグラフィー, 放射性医薬品, 18F-フルオロコリン, 18F-フルオロアミノ酸, 18F-FACBC, 脳, 乳腺, 前立腺, 腫瘍,リンパ節転移, アミノ酸代謝, コリン代謝,
diagnostic imaging, positron emission tomography, PET, radiopharmaceutical, 18F-fluoro-choline, 18F-fluoro-amono acid, brain, breast, prostate, tumor, lymph node metastasis, amino acid metabolism, choline metabolism
分類コード:030502, 030301, 030403
放射線利用技術データベースのメインページへ



