放射線利用技術データベースのメインページへ
作成: 2000/02/04 鷲野 弘明
データ番号 :030158
RI標識非ホジキンリンパ腫治療抗体
目的 :RI標識モノクローナル抗体を利用した非ホジキンリンパ腫治療剤の特徴の説明
放射線の種別 :ベータ線
応用分野 :医学、治療
概要 :
β線を放出する放射性同位元素(RI)で標識されたモノクローナル抗体が、新しいタイプの抗がん剤として開発されている。これは、体外から放射線を照射する従来の放射線療法と異なり、体内にRI標識抗体を投与し、体内から病変部を照射する治療法(放射免疫療法)である。非ホジキンリンパ腫は、放射線感受性が高い腫瘍で、放射免疫療法の有望な対象として研究されてきた。開発中の薬剤は、従来の抗がん剤が効かなくなった再発患者にも有効性が認められ、将来我が国でも利用が進むと期待される。
詳細説明 :
1. 非ホジキンリンパ腫とは
血液腫瘍には、白血病・骨髄腫・ホジキン病・非ホジキンリンパ腫など様々な腫瘍があり、形態学的、臨床的に分類される。非ホジキンリンパ腫(Non-Hodgkin's Lymphoma:NHL)はこのなかの一つのカテゴリーであり、NHLにはさらに腫瘍が由来する免疫細胞などに基づいた分類や、悪性度に基づき低度・中等度・高度群に分類する国際分類もある。
NHLは一般に30歳以上の成人で発生するが、エイズに関連した悪性腫瘍として最もよく見られる腫瘍のひとつでもある。日本のNHL患者発生率・発生数は、欧米に比べてかなり低い(日本:約4,000人/1992年国立がんセンター統計資料、米国:55,000人/1998年アメリカがん学会統計資料)。NHLは、一般に薬剤感受性や放射線感受性が高い。治療法は、NHLのタイプにより異なるものの、通常化学療法と放射線療法の組み合わせが選択される。NHLでは、治療後25〜30%の患者が寛解するといわれる。化学療法では、他の癌の場合と同様に薬剤耐性が問題となり(治療を継続するに従って薬剤耐性が発現する)、薬剤耐性となった進行期NHLの治療はもっとも難しい問題の一つと言える。
血液腫瘍の研究は、免疫系細胞や血液幹細胞の細胞膜表面抗原(表面マーカー)に特異的なモノクローナル抗体が作成されたことにより、飛躍的に進んだ。NHLは、骨髄系リンパ球(B細胞)の悪性化という共通の特徴をもち、B細胞に特徴的な表面マーカーを分化度に応じて発現する傾向がある。この結果、これらの抗体を治療に利用する、いわゆる免疫療法が考え出された。ここで紹介するのは、抗体自身の免疫学的作用に加え、それ自身が運搬する放射性同位元素(RI)が放出する放射線により、NHLを治療しようとする最新のRI標識モノクローナル抗体である。
2. RI標識モノクローナル抗体の治療メカニズム
放射線治療は、従来、放射性同位元素線源あるいは他の放射線照射装置を用いて体外から特定部位の患部に向けて放射線を照射するか、特定患部に放射性同位元素を含んだ小型器具を挿入留置しそこで照射するものであった。それに対し、ここで取り上げる放射線治療は、RIで標識された薬剤を体内に投与し、この薬剤が体内で存在する場所(病変部)をRIから放出される放射線で照射する、即ちミクロのレベルで内側から照射するものである。よって、標的病変への照射は、RIのキャリアーである薬剤の体内分布によって決定される。もし、化合物が病変部位に特異的に結合しそれ以外の正常組織に結合せず、かつ、放射線の飛程が非常に短かければ、高濃度に薬剤が存在する病変部位の放射線照射線量は、正常組織に比べて高くなる。実際、β線のエネルギーは、生体組織内では発生位置から飛程2〜3mm以内ですべて吸収される。
β線放出核種を運搬するモノクローナル抗体は、血中投与されると血流にのって全身に分布し、自分自身で癌細胞などを探してそこに安定的に結合する。これにより、癌組織は集中的に放射線照射を受け、一方、癌組織以外の正常組織はあまり照射されない。これが、RI標識モノクローナル抗体によるRI治療の基本コンセプトであり、薬物動態に基づく選択的放射線照射が最大の特徴である。この治療法のメリットは、体外から狙った場所以外照射できない体外照射法と違って、全身を対象に治療でき、診断では発見できなかった小さな病変ももらさず照射し得ることにある。
1980年代より、血液腫瘍・黒色腫・肺癌・乳癌・大腸癌などに選択的に結合するモノクローナル抗体を、I-131・Y-90・Ho-166・Lu-177・Re-186などのβ線放出核種で標識し、それを用いてがん細胞移植マウスで治療実験が行われた。1990年代に入り、特に高い治療効果が期待されたNHLで臨床試験が行われた。
3. 現在研究開発中のRI標識モノクローナル抗体製剤
RI標識モノクローナル抗体によるNHL治療は、すでに基礎研究段階から臨床試験段階へ移行している。現在開発中の製剤の状況を図1にまとめた。抗体は、現時点ではマウス型抗体が使われているが、将来的にはヒト型化抗体に移行すると考えられる。使用される放射性核種は、β線エネルギーと放出効率、同時に放出されるγ線の有無及びそのエネルギー・放出効率、物理的半減期、生産性(生産量・コスト)、標識技術など、様々な要素を勘案して決定される。目下、I-131とY-90が利用されている。図1中の臨床試験結果の簡単な紹介は、開発を行っている各社のホームページや文献報告より引用した。
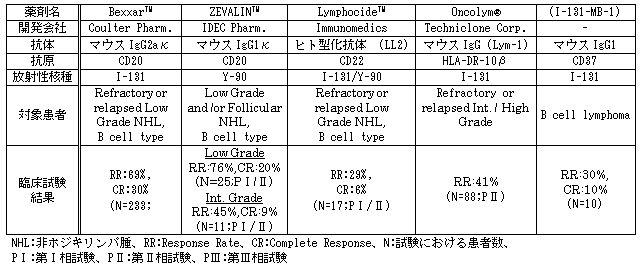
図1 現在 上市〜開発中のNHL治療用標識モノクローナル抗体
4. 131I-抗CD20抗体による低悪性度NHLの治療成績
低悪性度NHLは、限局期にある間治療成績は悪くない。しかし、低悪性度でも進行期に至れば、薬剤耐性の獲得とともに再発を繰り返すようになり、根治は困難となる。5年生存率は、低悪性度全体で見ると50〜70%だが、進行期患者の無病生存率(disease-free survival rate)だけ見ると5%以下と言われる。中悪性度NHLでは、化学療法(CHOP療法)と放射線療法が主体で、約80%の患者が長期の寛解を得る。しかし、再発した場合やがて進行期に至り、薬剤耐性が同様に問題となる。中悪性度NHL全体の5年生存率は、35〜45%と推測される。
いくつかの抗がん剤を組み合わせるCHOP療法は既に古典的といえ、それに代わる化学療法が研究されたが、目下これを凌ぐものは見出されていない。進行期の患者に対しては有効な治療法がないといえる。このような状況の中で、RI標識モノクローナル抗体が登場した。
Liuらは、I-131標識抗CD20モノクローナル抗体(131I-B-1抗体)の治療効果を、薬剤耐性となり化学療法が適用困難となった進行期NHL患者29例を対象に研究した。まず、治療開始前に本剤を各患者に少量(185〜370 MBq)投与し、イメージングを行って、本剤が正常臓器や骨髄に与える放射線量(吸収線量)を患者ごとに推定した。この薬剤は自家骨髄移植を前提としているため、骨髄以外で放射線量が問題となるのは肺であった。そこで、各患者の肺吸収線量が25〜31Gyの間に入るよう薬剤投与量が決定された。その投与量における腫瘍吸収線量は、患者平均で38±12Gy、全身線量は同じく4.1±1.4Gyであった。こうして、各患者に治療量の131I-B-1抗体を投与した。投与量は27例の患者で1.7mg/kg抗体とし、放射能量としては10.4〜29.0GBqであった。これらの患者は、その後すべて自家骨髄移植を受けた。治療後の成績を図2に示す。左の図は、対象患者全体の生存率をoverall(全生存率)とprogression-free(NHL非再発生存率)で示したのもである。右の図は、今回の結果をこの患者群が過去に経験した治療の結果と対比させてある。Aの線は今回得られた非再発生存率(progression-free survival)で、Bはこの患者群が過去の治療で経験した最も長い治癒期間から考えられる生存確率(survival probability)、Cは今回の治療に入る直前の治療で得られた治癒期間から考えられる生存確率である。
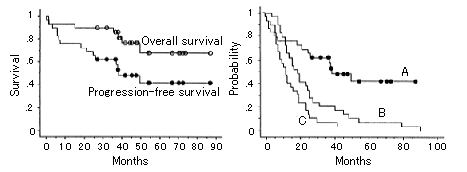
図2 I-131標識抗CD20モノクローナル抗体(131I-B-1抗体)によるNHL患者の治療 (原論文1より引用。 Reproduced from J.Clin. Oncol., vol.16, p.3270-3278, 1998, Figures 2,3 (p.3273), S.Y.Lie, J.F.Eary, S.H.Petersdorf, et al., Follow-up of relapsed B-cell lymphoma patients treated with Iodine-131-labeled anti-CD20 antibody and autologous stem-cell rescue, Copyright(1998), with permission from Lippincott-Raven Publishers.)
右側の図から推測されるように、もしこれら29例の患者に131I-B-1抗体治療を行わなければ、3年後の生存確率は10%以下と予測されるが(C)、治療を実施することで7年後に至るも40%以上の生存率が確認できた。これら進行期NHL患者には何ら治療法がない現状では、この成績は十分注目すべきものである。
コメント :
RI標識モノクローナル抗体による癌治療は、放射線治療の可能性を広げる新たな治療法として注目される。しかし、大きな固形癌にはあまり治療効果は期待できない、骨髄照射による血液毒性など、いくつかの問題点を指摘し得る。今後の研究開発が望まれる。
原論文1 Data source 1:
Follow-up of relapsed B-cell lymphoma patients treated with Iodine-131-labeled anti-CD20 antibody and autologous stem-cell rescue
S.Y.Lie, J.F.Eary, S.H.Petersdorf, et al.
J.Clin. Oncol., vol.16, p.3270-3278, 1998
参考資料1 Reference 1:
Iodine-131-Anti-B1 radioimmunotherapy for B-cell lymphoma
M.S.Kaminski, K.R.Zasadny, I.R.Francis et al.
J. Clin. Oncol., vol.14, p.1974-1981, 1996
参考資料2 Reference 2:
Radioimmunotherapy of relapsed Non-Hodgkin's lymphoma with Zevalin, a 90Y-labeled anti-CD20 monoclonal antibody
G.A.Wiseman, C.A.White, T.E.Witzig et al
Clin. Cancer Res(suppl.). vol.5, p.3281s-3286s, 1999
参考資料3 Reference 3:
Treatment of Non-Hodgkin's lymphoma with radiolabeled murine, chimeric or humanized LL2, an anti-CD22 monoclonal antibody
M.Juweid, R.M.Sharkey, A.Markowitz et al.
Cancer Research(suppl.) vol.55, p.5899s-5907s, 1995
参考資料4 Reference 4:
Factors affecting 131I-Lym-1 pharmacokinetics and radiation dosimetry in patients with Non-Hodgkin's lymphoma and chronic lymphocytic leukemia
G.L.DeNardo, S.J.DeNardo, S.Shen et al.
J. Nucl. Med. vol.40, p.1317-1326, 1999
参考資料5 Reference 5:
Imaging, dosimetry, and radioimmunotherapy with iodine 131-labeled anti-CD37 antibody in B-cell lymphoma
M.S.Kaminski, L.M.Fig, K.R.Zasadny et al.
J. Clin. Oncol. vol.10, p.1696-1711, 1992
キーワード:放射免疫治療 radioimmunotherapy, 放射性医薬品 radiopharmaceutical, モノクローナル抗体 monoclonal antibody, 腫瘍 tumor, 悪性リンパ腫 malignant lymphoma, 非ホジキンリンパ腫 non-Hodgkin's lymphoma, ベータ核種 beta-emitter, 白血球膜抗原 leukocyte cell membrane antigen, B細胞リンパ腫 B-cell lymphoma, CD20, CD22
分類コード:030502, 030301, 030403
放射線利用技術データベースのメインページへ
