放射線利用技術データベースのメインページへ
作成: 1999/01/4 鷲野 弘明
データ番号 :030118
腫瘍シンチグラフィー用モノクローナル抗体診断剤-1:Technetium(Tc-99m) Arcitumomab注射液(CEA-Scan)
目的 :モノクローナル抗体を利用した大腸癌・直腸癌診断剤の特徴の説明
放射線の種別 :ガンマ線
応用分野 :医学、診断
概要 :
Technetium(99mTc) Arcitumomab注射液は、腫瘍胎児抗原(CEA)に特異的に結合するマウス型モノクローナル抗体IMMU-4のFab'フラグメントを有効成分とし、用時99mTc標識される診断用放射性医薬品である。CEAは大腸癌や直腸癌などで高頻度に発現するため、本注射液によるこれらの癌の診断は、CTなどでは確定できない病変の評価及びその後の治療方針決定に有用である。なお、本剤は我が国では販売されていない。
詳細説明 :
腫瘍とは、細胞増殖に関与する遺伝子の異常が主な原因で不死化した細胞集団であり、様々な組織より発生する。腫瘍は、正常組織では見られない抗原をしばしば発現し、これらは腫瘍関連抗原と呼ばれる。ヒト腫瘍組織を他の動物に接種・感作させると、腫瘍抗原に結合する抗体を作成することができる。例えば、マウスをヒト腫瘍組織で感作したのち、抗体を産生するプラズマ細胞を取り出して骨髄腫細胞と融合し、腫瘍に特異的な抗体を産生する融合細胞をクローニングすると、腫瘍抗原にのみ結合する抗体(モノクローナル抗体)を大量に作製できる。
1970年代末にモノクローナル抗体を作製する技術が開発されると、放射性同位元素で標識した抗体を腫瘍の核医学診断に応用する試みが直ちに始まった。1980年代には抗体イメージング剤の研究が盛んに行われ、1990年代にはいくつかの製剤が米国で販売されるに至った。ここでは、それらのうち米国Immunomedics社のTechnetium(99mTc) Arcitumomab注射液(CEA-ScanTM、以下本注射液)を紹介する。現在のところ、本注射液は我が国では販売されていない。
Arcitumomabは、腫瘍胎児抗原(carcinoembryonic antigen;CEA)に特異的に結合するマウス型モノクローナル抗体IMMU-4のFab'フラグメントを有効成分とし、用時99mTc標識できるよう調製された製剤である。CEAは大腸癌や直腸癌などで高頻度に発現するため、Technetium(99mTc) Arcitumomab注射液は、CTなどでは確定できない病変の評価及びその後の治療方針決定に有用である。
テクネチウム-99m(99mTc)は、原子炉で生産される99Moより生成する物理的半減期6.01時間の放射性核種で、β線を放出せず、放出γ線のエネルギーは140.5keVでシンチグラフィーに適している。
1. 99mTc-Arcitumomab注射液の組成
Arcitumomabは、用時99mTc標識して使用する標識用キットで、凍結乾燥バイアルとして供給される。バイアルには、Arcitumomab 1.25mg、SnCl2 0.29 mg及び酒石酸カリウム・ナトリウム、酢酸ナトリウム、塩化ナトリウム、しょ糖などの添加物が含まれる。
用時、本バイアルに過テクネチウム酸ナトリウム(99mTc)注射液を添加溶解し、注射液を調製する。
2. 99mTc-Arcitumomab注射液の効能又は効果
大腸癌、直腸癌の診断。
本注射液は、これらの癌が組織診断で証明された患者において、通常の診断法に加えて本注射液による画像診断を行い、肝臓・肝臓以外の腹腔内及び骨盤腔内における浸潤・転移・再発を検出する。本注射液は、血清中CEA値の上昇や通常診断で癌の再発が疑われながら、その存在部位を確定できない(=癌が証明できない)患者にも適用される。
3. 99mTc-Arcitumomab注射液の用法及び用量
Arcitumomabバイアルに、過テクネチウム酸ナトリウム注射液(1.11 GBq/ml)を1 ml加えて30秒ほどよく振り溶解する。標識反応は、室温5分程度で完了する。標識後、本注射液に生理食塩液1 mlを加えて希釈し、放射化学的純度を薄層クロマトグラフィーで測定して純度が90 %以上あることを確認する。
通常、成人に推奨される投与量は740 MBq〜1.11 GBq/1mg Arcitumomab/2 mlであり、肘静脈より投与する。必要に応じて30 mlの生理食塩液で希釈し、5〜20分ほどかけ点滴静注しても良い。投与2〜5時間後にガンマカメラあるいはSPECT装置で被験部を撮像する。必要に応じて、投与後24時間までに局所像を得る。
4. 99mTc-Arcitumomab注射液の薬効薬理
CEAは、胎生期に消化器系組織で見られるが、成人正常組織ではもはやほとんど発現せず、癌・クローン病・炎症性消化器疾患などで発現する。CEAは腫瘍関連抗原の一つとして良く知られ、様々な癌特に消化器系の癌組織で発現することが分かっている。CEAは、これらの疾患で発現されると血液中に出現する。血清CEA値からこうした疾患の存在を診断できるが、その部位を特定することはできない。従って、本注射液を用いて画像診断することにより、その部位の特定が可能となり、治療方針決定に役立つ。
Arcitumomabは、CEAに特異的に結合するマウス型モノクローナル抗体(IgG1) IMMU-4 のFab'フラグメントで、分子量約50 kDaの蛋白質である(図1参照)。IMMU-4は、細胞膜上に発現する200 kDaの古典的CEAに特異的に結合する抗体である。
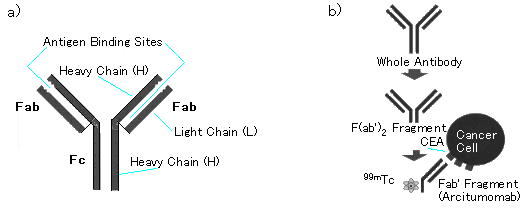
図1 99mTc-Arcitumomabの推定構造。
IgGは、二つのheavy chainと二つのlight chainがSS結合でつながった構造をしている。このうち、Fcフラグメント部分は抗体分子から切り離しても、抗体が抗原に結合する力は影響を受けない。99mTc-Arcitumomabは、酵素的切断によりFab'を取り出し、99mTcで標識したものである.(原論文1より引用)
5. 99mTc-Arcitumomab注射液の体内動態
静脈内投与後の血液中放射能は、投与後1、5及び24時間で各々投与量の63 %、23 %及び7 %であった。投与初期の血中消失半減期は約1時間であり、体外排泄半減期は13±4時間であった。投与後24時間までに、投与放射能の約28 %が尿中に排泄された。
6. 99mTc-Arcitumomab注射液の臨床適用
本注射液は、米国で大腸癌及び直腸癌を対象に実施された臨床試験においてその有用性が示された。第III相試験の成績(integrated assessment in phase III)は、以下のとおりである:
CEA-Scan 腹腔内 肝臓 骨盤腔 全体
sensitivity 46 %(44/96) 63 %(132/211) 60 %(62/103) 57 %(240例/419例)
specificity 85 %(95/112) 90 %(96/107) 74 %(69/93) 83 %(262例/314例)
以下に臨床例を示す。
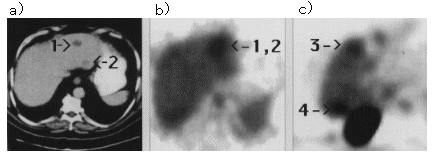
図2 大腸癌の肝臓転移の例。
この患者は、20年前に結腸癌で治療を受けたが、さらに大腸癌が発見され手術を受けた。その後肝臓への転移が明らかとなり、CT及びCEA-Scanによるイメージングを行った。CTでは、肝の右葉に2ヶ所転移が発見された(<-1、<-2)。一方、CEA-Scanでは、さらに左葉に二ヶ所(<-3、<-4)発見された。これら4ヶ所は、いずれも手術で切除され、病理検査で腫瘍と確認された。(原論文1より引用)
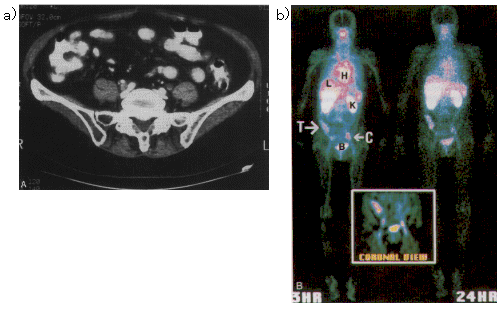
図3 大腸癌の局所再発の例。
この患者は、S字結腸〜直腸に癌が発見され、手術及び放射線治療などを受けた。5年後に血液中のCEAレベルが14 ng/mlに上昇し、再発を疑われてCT検査を行なったが、CT像に示したように腫瘍は発見されなかった。そこでCEA-Scanによる検査を行ない、腹腔内の二ヶ所で腫瘍の再発が発見された(T,C)。(H:心臓、L:肝臓、K:腎臓、B:膀胱) (原論文2より引用。 Reproduced from Data source 2 copyrighted in 1997 by Annals of Surgery, vol.226 No.5, p.621-631, 1997; Figure 1 (p.626).)
7. 99mTc-Arcitumomab注射液の副作用
Arcitumomabは、ヒトにとって異種蛋白質であるため、これを体内に投与すると抗体が産生され得る。本注射液では、Fab'フラグメントを用いることにより、このヒト抗マウス抗体(HAMA)の産生を最小限に抑えている。臨床試験では400例以上の患者でHAMA検査を行い、HAMAが検出された割合は1%以下であった。
臨床試験(500例以上)では、本注射液に関連すると見られる副採用が報告されたのは1例であった。その他には、軽いめまい、頭痛、発熱などが1例ずつ認められた。
コメント :
腫瘍診断剤としては他にクエン酸ガリウム(67Ga)注射液があるが、これは大腸癌・直腸癌の診断には使用できない。
原論文1 Data source 1:
Introduction to CEA-ScanTM : Arcitumomab Imaging of Recurrent & Metastatic Colorectal Cancer
Yehuda. Z. Patt, Steven. M. Larson, Richard. L. Wahl & David. M. Goldenberg
Immunomedics, Inc.
Nuclear Medicine & Radiology Update Series、1998年5月28日版
原論文2 Data source 2:
Use of carcinoembryonic antigen radioimmunodetection and computed tomography for predicting the resectability of recurrent colorectal cancer
K. Hughes, C. M. Pinsky, N. J. Petrelli, F. L. Moffat, Y. Z. Patt, L. Hammershaimb & D. M. Goldenberg
Annals of Surgery, vol.226 No.5, p.621-631, 1997
キーワード:画像診断, 放射性医薬品, 免疫シンチグラフィー, モノクローナル抗体, 腫瘍, 浸潤, 再発, CEA-Scan, 腫瘍胎児抗原, 大腸癌, 直腸癌, 腹腔内転移, 肝転移, リンパ節転移
diagnostic imaging, radiopharmaceutical, radioimmunoscintigraphy, monoclonal antibody, tumor, invasion, recurrence, Technetium(99mTc) Arcitumomab, carcinoembryonic antigen, CEA, colorectal cancer, abdominal metastasis, liver metastasis, lymphnode metastasis
分類コード:030502, 030301, 030403
放射線利用技術データベースのメインページへ

