放射線利用技術データベースのメインページへ
作成: 1999/01/09 斎藤 恭一
データ番号 :010156
放射線グラフト重合法で作成した高分子界面への微生物細胞の吸着
目的 :黄色ブドウ状球菌を捕捉するための高分子材料の開発
放射線の種別 :電子
放射線源 :電子加速器
線量(率) :200 kGy
利用施設名 :日本原子力研究所高崎研究所2号加速器
照射条件 :窒素雰囲気、室温
応用分野 :医薬品工業、食品工業
概要 :
ポリエチレンに電子線を照射後、エポキシ基をもつモノマーを重合した。その後、ジエチルアミンとの反応によってジエチルアミノ基を導入した。こうしたプラスの電荷をもつグラフト高分子鎖の柔らかい界面にマイナスの表面電荷をもつ微生物細胞が衝突すると、多点で静電的相互作用が確実に働いて微生物細胞が界面に捕まる。したがって、捕捉速度定数はプラスの電荷をもっていてもグラフト高分子鎖をもたない界面のそれに比較して約1、000倍になった。
詳細説明 :
微生物細胞の表面はマイナスの電荷を帯びている。微生物はグラム陰性菌(例えば、大腸菌)とグラム陽性菌(例えば、黄色ブドウ状球菌)とに分類される。ここでは、表面マイナス電荷密度の高い黄色ブドウ状球菌を、プラスの電荷を与えるイオン解離性基(ジエチルアミノ基)をもつグラフト高分子鎖で捕捉することを提案する。
中空糸状ポリエチレン多孔性膜に、電子線をあてて、エポキシ基をもつモノマー(グリシジルメタクリレート)をグラフト(接ぎ木)した。さらにその後、グラフト高分子鎖中のエポキシ基にジエチルアミンを反応させると、エポキシ基をジエチルアミノ基へ変換できる。微生物細胞は膜の孔より大きいので、微生物細胞懸濁液中で微生物細胞は孔に侵入できずに中空糸膜の外部表面にひっかかる。
表面にマイナス電荷をもつ微生物細胞は、プラスの電荷にひっぱられて接近し衝突する。衝突したからといって微生物細胞が捕捉されるかどうかは別問題である。グラフト高分子鎖をもつ界面は柔らかいので、微生物細胞がプラス電荷と多点で接触しやすく、微生物細胞が衝突すると離れず捕捉されやすいと期待される。
黄色ブドウ状球菌懸濁液に中空糸膜を投げ入れてしんとうした。懸濁液中の黄色ブドウ状球菌の濃度の経時変化を追跡した。懸濁液中の菌数の減衰速度は一次反応モデル(減衰速度が濃度に比例するということ)で近似できた。ここで、材料の外部表面積を考慮して捕捉速度定数を算出した。
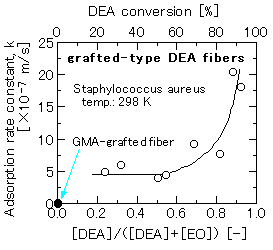
図1 Relationship between the adsorption rate constant of S. aureus and the mole fraction of DEA of the grafted-type DEA fibers.(原論文1より引用。 Reproduced with permission from Biotechnol. Prog., 12, 178-183(1996), Fig.4(p.181), William Lee, Shintaro Furusaki, Kyoichi Saito, Takanobu Sugo, Keizo Makuuchi, Adsorption kinetics of microbial cells onto a novel brush-type polymeric material prepared by radiation-induced graft polymerization;Copyright(1996), American Chemical Society. )
グラフト高分子鎖中のジエチルアミノ基密度が増加するとともに捕捉速度定数が増した(図1)。エチレングリコールジメタクリレートで架橋したグリシジルメタクリレートビーズにジエチルアミノ基を導入した界面を作成し比較した。
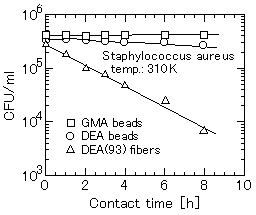
図2 Comparison of adsorption rate between the DEA beads and DEA fibers.(原論文1より引用。 Reproduced with permission from Biotechnol. Prog., 12, 178-183(1996), Fig.5(p.181). )
両方の材料を使って、同一条件下で同様の実験をおこない、捕捉速度定数を比較した。「非グラフト高分子鎖」界面に比べて、「グラフト高分子鎖」界面の捕捉速度定数は約1、000倍であった(図2)。表面にマイナスの電荷をもつ微生物細胞が、プラスの電荷をもつ柔らかいグラフト高分子鎖からなる界面に多点で衝突捕捉されることによって、同一のイオン解離性基密度をもつ堅い界面に比べて、より確実に捕捉されると推察される。

図3 SEM images of the interfaces of DEA beads and DEA fibers before adsorption and after S. aureus cell suspension was brought into contact for 8 h.(原論文1より引用。 Reproduced with permission from Biotechnol. Prog., 12, 178-183(1996), Fig.6(p.181).)
黄色ブドウ状球菌を捕捉した材料の表面を走査型電子顕微鏡(SEM)を使って観察する(図3)と、「グラフト高分子鎖」界面では、黄色ブドウ状球菌はほとんど変形していなかったのに対して、「非グラフト高分子鎖」界面では、黄色ブドウ状球菌は張り付いたように平たくなってしまっていた。
コメント :
放射線グラフト重合法で作成したグラフト高分子鎖の長さが1ミクロン以上であることを利用して、同程度のサイズの微生物細胞を確実に、言い換えれば、速く捕捉しようというアイデアからこの研究は始まっている。これまでの材料に比べて1、000倍ほども捕捉速度定数が大きくなったと報告している。しかしながら、捕捉した細胞の生物活性の変化についての記述がない。用途開発のために、今後こうした評価が必要である。殺菌用なのか、または細胞固定化用なのか、材料のニーズを明確にしていくことが望まれる。
原論文1 Data source 1:
Adsorption kinetics of microbial cells onto a novel brush-type polymeric material prepared by radiation-induced graft polymerization
William Lee, Shintaro Furusaki, Kyoichi Saito, Takanobu Sugo, Keizo Makuuchi
Univeristy of Tokyo, Chiba University, JAERI (Takasaki Radiation Chemistry Research Establishment)
Biotechnol. Prog., 12, 178-183(1996)
原論文2 Data source 2:
Capture of microbial cells on brush-type polmeric matrials bearing different functional groups
William Lee, Shintaro Furusaki, Kyoichi Saito, Takanobu Sugo
Univeristy of Tokyo, Chiba University, JAERI (Takasaki Radiation Chemistry Research Establishment)
Biotechnol. Bioeng., 53, 523-528(1997)
キーワード:放射線グラフト重合法、イオン解離性基、エポキシ基、高分子ブラシ、黄色ブドウ状球菌細胞、大腸菌細胞、捕捉、捕捉速度定数
radiation-induced graft polymerization, ionizable group, epoxy group, polymer brush, staphylococcus aureus cell, Escherichia coli cell, capturing, capturing rate constant
分類コード:010201, 010203, 010401
放射線利用技術データベースのメインページへ

