放射線利用技術データベースのメインページへ
作成: 1998/12/15 斎藤 恭一
データ番号 :010153
放射線グラフト重合法によって作成した不斉加水分解用固定化酵素膜
目的 :不斉加水分解酵素を固定した高活性な多孔性中空糸膜の作成と評価
放射線の種別 :電子
放射線源 :電子加速器(3MeV,25mA)
線量(率) :200 kGy
利用施設名 :日本原子力研究所高崎研究所2号加速器
照射条件 :窒素気流中、室温
応用分野 :酵素工学、食品工学、光学分割、固定化技術
概要 :
多孔性中空糸膜の孔表面にアニオン交換基をグラフトした高分子膜を放射線グラフト重合法、それに続く官能基導入反応によって導入し、そこへ酵素アミノアシラーゼを積層吸着させ、さらにグルタルアルデヒドで分子間を架橋した。この膜に、光学異性体アセチル-DL-メチオニン溶液を透過させて不斉加水分解活性を評価した。この方法は従来のアミノアシラーゼ固定ビーズ充填カラム法に比べ、低い操作圧力で高い空間速度が得られる点および転化率が高い点で有利である。
詳細説明 :
医薬、食品分野では、光学異性体を分離し、有用な一方の光学異性体を分取する技術の必要性が高まっている。光学異性体の一方を選択的に加水分解する機能(不斉加水分解能)を有する酵素アミノアシラーゼを固定化したバイオリアクターを用いて利用価値の高いL -アミノ酸を生成させる方法について、多くの研究が行われている。
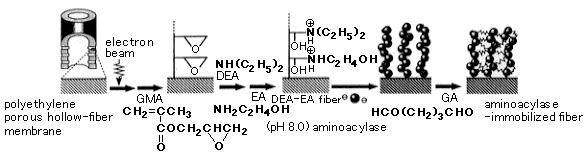
図1 Preparation scheme of aminoacylase-multilayered porous hollow-fiber membrane(原論文1より引用)
本研究で提案する膜の作成経路を図1に示す。(1)基材膜であるポリエチレン製の多孔性(平均細孔径0.4 ミクロン)中空糸膜に電子線を照射してラジカルを生成させた後、グリシジルメタクリレート(GMA)/メタノール溶液に浸した。基材膜に対して重量が2倍のGMAグラフト重合膜を作成した。(2)GMAグラフト重合膜をジエチルアミン、つぎにエタノールアミンに浸して、ジエチルアミノ(DEA)基および2-ヒドロキシエチルアミノ(EA)基を導入した。(3)得られたDEA-EA膜の内面から外面へアミノアシラーゼ溶液を透過させ、膜にアミノアシラーゼをイオン交換吸着させた。(4)アミノアシラーゼ吸着膜をグルタルアルデヒド溶液に浸して、膜に吸着したアミノアシラーゼ分子間を架橋した。
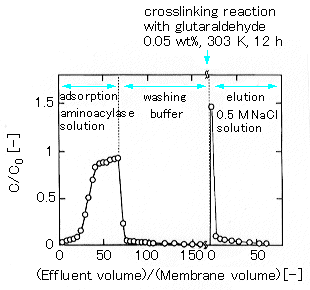
図2 Breakthrough curve of aminoacylase through the DEA-EA fiber and elution curve of aminoacylase after crosslinking reaction(原論文1より引用)
DEA-EA膜にアミノアシラーゼ溶液を透過させたときの破過曲線と、架橋反応後の溶出曲線を図2に示す。破過曲線から膜へのアミノアシラーゼの吸着量を求めると、膜1グラムあたり108 mgであった。また、グルタルアルデヒドを用いた架橋反応とそれに続く0.5 M NaCl溶液を用いた溶出後の膜へのアミノアシラーゼの架橋固定量は、膜1グラムあたり81 mgであった。膜1mLあたり33 mgにあたる。DEA-EA膜の比表面積とアミノアシラーゼの理論単層吸着量とから、得られた膜へのアミノアシラーゼの架橋固定量は、約7層の積層(多層吸着)にあたる。
アミノアシラーゼ架橋固定膜にリン酸緩衝液を透過させたときの通液空間速度(流量を膜体積で割った値、SV)は操作圧力に比例し、0.03 MPaの操作圧力下でSVは150 h-1に達した。既存のアミノアシラーゼを固定したビーズ充填カラム法ではSV は10 〜40 h-1で操作されている。アミノアシラーゼ架橋固定膜は、低い操作圧力で高いSVが得られることが確認できた。
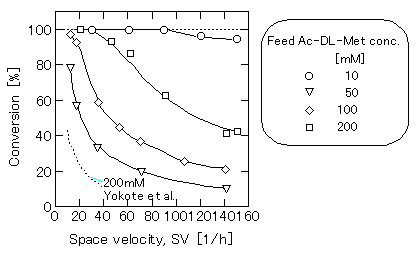
図3 Conversion from Ac-L-Met into L-Met by an aminoacylase-immobilized fiber as a function of the space velocity(原論文1より引用)
アミノアシラーゼ架橋固定膜にアセチル-DL-メチオニン溶液を透過させたときの転化率のSVによる変化を図3に示す。基質濃度が10 mM では、SV = 90 h-1 までは転化率は 100%であった。しかしながら、どの基質濃度でもSVが高くなるにつれて転化率が低下した。この結果は、アミノアシラーゼをアミノ基を有するガラスビーズにグルタルアルデヒドによって共有結合で固定したビーズ充填カラム(アミノアシラーゼ固定量はガラスビーズ1mLあたり8〜31mg)での結果と同様の傾向となった。これは、高SV では基質の供給が過剰で、加水分解反応が十分に進行しないうちに基質が膜を透過してしまうことを示している。同じ条件(基質濃度200 mM)で、膜とガラスビーズカラムの転化率を比べると、膜を用いる本研究の方法が約2倍高いことがわかった。
以上よりグラフト高分子鎖を導入した多孔性中空糸膜にアミノアシラーゼを多層で固定した膜をバイオリアクターとして利用できることがわかった。この方法は、従来のビーズ充填カラム法に比べ、低い操作圧力で高い空間速度が得られる点および転化率が高い点で有利である。
コメント :
酵素を固体に固定することによって、酵素反応後に酵素と反応生成物とを分ける手間を省くことができ有利である。これまで研究が多くなされてきた割には、固定化酵素の実用化例が少ない。本研究は、固定化酵素を利用した実用反応例としてアミノアシラーゼによるアセチル-DL-メチオニンの不斉加水分解を扱っている。田辺製薬が開発した固定化担体がビーズであるのに対して、この研究が提案している担体は多孔性中空糸膜である。多孔性膜の内面から外面に均一に酵素固定用の高分子鎖を取り付ける手法として放射線グラフト重合法が利用されている。両者の活性を比較すると、アミノアシラーゼ固定化多孔性中空糸膜が優れている。ここでの手法は、センサーあるいは診断材料の開発に応用できる。
原論文1 Data source 1:
アミノアシラーゼ多層架橋固定膜のバイオリアクターへの応用
中村昌則、斎藤恭一、杉田和之、須郷高信
千葉大学、日本原子力研究所高崎研究所
膜 23,pp316-321(1998)
キーワード:放射線グラフト重合法、多孔性中空糸膜、アミノアシラーゼ、アセチル-�DL-メチオニン、固定化酵素、グルタルアルデヒド、分子間架橋、加水分解
radiation-induced graft polymerization, porous hollow-fiber membrane, aminoacylase, acethyl-DL-methionine, immobilized enzyme, glutaraldehyde, crosslinking, hydrolysis
分類コード:010201, 010202
放射線利用技術データベースのメインページへ

