作成: 1998/12/18 吉田 勝
データ番号 :010150
製剤針からの制癌剤のin vivo放出
目的 :制癌剤を徐放する製剤針の開発とその応用
放射線の種別 :ガンマ線
放射線源 :60Co線源(104MBq)
線量(率) :25kGy
利用施設名 :日本原子力研究所高崎研究所コバルト棟
照射条件 :窒素気流中、ドライアイス温度
応用分野 :癌の治療
概要 :
シスプラチン制癌剤を含むコポリマー製剤針を低温放射線重合技術を用いて調製した。この製剤針をラットの腎臓に埋め込み、制癌剤のin vivo 放出を調べた。その結果、埋め込みから70日後に、制癌剤は完全に放出した。また、壊死範囲を埋め込みの14日目で観察したところ、600-3100μmであった。
詳細説明 :
シスジクロロジアミン白金(II)(シスプラチン)を含む製剤針の調製スキームを図1に示す。
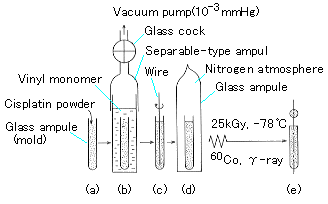
図1 Scheme for the preparation of a needle-type copoly(2G/14G, 80/20 vol. %) formulation containing 6 mg of cisplatin.(原論文1より引用。 Reproduced from Biomaterials, Vol. 10, Pages 16-22 (1989), Fig.2(p.17), Masaru Yoshida, Masaharu Asano, Yasuhi Morita, Isao Kaetsu, Kyoichi Imai, Tooru Mashimo, Hisako Yuasa, Hidetoshi Yamanaka, Umeko Kawaharada, and Keiji Suzuki, In Vivo Release of Cisplatin from a Needle-Type Copolymer Formulation Implanted in Rat Kidney; Copyright(1989), with permission from Elsevier Science.)
内径0.8mmのガラスアンプル鋳型にシスプラチン粉末を充填、次いで、この鋳型を液状モノマーを含むアンプル中に浸した。液状モノマーは、ジエチレングリコールジメタクリレート(2G)とテトラデカエチレングリコールジメタクリレート(14G)の混合系からなる。真空脱気によって、モノマーを鋳型の中に十分に浸透、さらに、シスプラチン粉末を液状モノマー中に均一に分散させるため、0.1 mm径のタングステン線でかき混ぜた。モノマーの重合は、窒素雰囲気中、-78℃(ドライアイス/エタノール系)、25kGy(10kGy/h)まで照射することにより行った。鋳型を剥離後、製剤針を6mm 長さにカットした。この製剤針に含まれるシスプラチンは6mg であった(ポリマーは3mgである)。
製剤針からのシスプラチンのin vivo放出は、ラットの腎臓に埋め込むことにより評価した。7日毎に屠殺したラット腎臓から製剤針を摘出、次いで、摘出した製剤針を蒸留水中に浸し、制癌剤を完全に水溶液中に溶出させた。溶液中の制癌剤濃度は、UV分光光度計(310 nmの吸光度)で測定した。この値から、製剤針中に残存している制癌剤濃度を求め、次いで、放出量を算出した。この放出量から、in vivo放出速度を求めた。
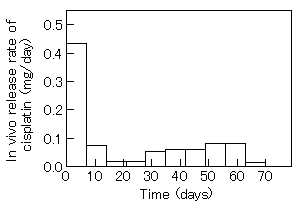
図2 Daily dose of cisplatin released from formulation containing cisplatin, implanted into rat kidney. The implanted formulation was collected from rat kidney at 7-d intervals.(原論文1より引用。 Reproduced from Biomaterials, Vol. 10, Pages 16-22 (1989), Fig.7(p.19), with permission from Elsevier Science. )
図2から明白なように、シスプラチンのin vivo放出速度は、最初の一週間、バーストのため非常に高い値を示すことが分かった(0.44mg/day)。その後、埋め込みから70日目で放出が完了するまで制癌剤は、0.01-0.08mg/dayの速度で放出した。このようなin vivo放出速度は、X線マイクロアナライザーでも測定が試みられている。所定時間毎にラットの腎臓から摘出した製剤針を輪切りにした。シスプラチンは、白金を含む化合物のため、X線マイクロアナライザーによる検出が可能である。エックス線像とラインプロフィールの結果から、製剤針中に制癌剤が残っている部分と放出した部分は、明確に区別できることが判明した。面積比から、in vivo放出速度を求めたところ、UV分光法で得た結果と良く一致することが分かった。この研究に用いたポリマーは、poly(2G-co-14G, 80/20 vol.%) からなり、含水率は37℃で4.8%であった。従って、水溶性のシスプラチンが、長期間にわたって徐放機能を維持できたのは、材料の疎水性、製剤針と接触していた腎組織の壊死化などに因るものと思われる。
表1 Changes in area of necrotized tissue surrounding a needle-type copoly(2G/14G, 80/20 vol. %) formulation containing 6 mg of cisplatin which was implanted into a left side of kidney of rats.(原論文1より引用。 Reproduced from Biomaterials, Vol. 10, Pages 16-22 (1989), Tab.1(p.21), with permission from Elsevier Science.)
-----------------------------------------------------------------------------------------
Cisplatin-containing copolymer Implantation Thickness of necrotized
formulation period tissue layer (μm)
No. ----------------------------------- (days) -----------------------------------
Composition (mg) Size (mm) Necrotic tissue Necrobiotic tissue
----------------- ---------------- (Dx) (Dy)
2G/14G Cisplatin Diameter Length
-----------------------------------------------------------------------------------------
1 3 600 600
2 7 1100 700
3 14 3100 600
4 21 2500 650
5 3 6 0.8 6 28 2000 600
6 35 1400 500
7 42 1000 600
8 56 600 600
9 63 400 500
10 70 300 500
11 9 0 0.8 6 7 - -
-----------------------------------------------------------------------------------------
Dx and Dy refer to the symbols given in Figure 13.
製剤針から腎組織内に放出されたシスプラチンの拡散範囲は、病理組織学的に調べられており、表1に結果を示す。腎組織が壊死化する範囲は、中心部の製剤針から円状に広がり、埋め込みから21日目で最大になる。この壊死は2種類からなる。すなわち、製剤針の周囲に出現する凝固壊死(necrosis)と凝固壊死の外側に見られる融解壊死(necrobiosis)である。凝固壊死の広がりは、中心部の製剤針から3,100μmにまで到達した。その後、この凝固壊死の広がりは、70日目で800μmに至るまで、経時的に減少することが分かった。これは壊死を起こした組織が、周りの正常細胞によって貪食を受けるためである。一方、融解壊死の場合、この壊死の広がりは、経時的に変化せず、500-700μmの値を示した。
制癌剤を含む製剤針を局所に埋め込むことによるラットの体重変化も調べられている。実験を始める前のラットの体重は420gである。制癌剤を含まない製剤針を埋め込んだ場合、体重は、実験開始から70日目で144%にまで増加することが分かった。これに対し、制癌剤を含む製剤針の場合、この値は119%であった。体重の減少は認められなかったが、制癌剤の作用によって体重の伸びが抑制される傾向を示した。
コメント :
制癌剤による壊死は、70日にわたる徐放性にも関わらず、最大で6,100μmの比較的に狭い範囲にしか及ばないことから、局所療法に適用するための製剤針として期待がもてる。この場合、乳癌、皮膚癌などの固形癌をもつ患者に対して、術前治療に有効である。しかしながら、用いたポリマーが生体で分解しないことから、術前に癌細胞を十分に委縮させ、委縮した癌細胞と一緒にポリマーを摘出することが望ましい。また、将来、生体で分解するポリマーによる制癌剤を含む製剤針の合成が必要である。
原論文1 Data source 1:
In Vivo Release of Cisplatin from a Needle-Type Copolymer Formulation Implanted in Rat Kidney
Masaru Yoshida, Masaharu Asano, Yasuhi Morita, Isao Kaetsu, Kyoichi Imai, Tooru Mashimo, Hisako Yuasa, Hidetoshi Yamanaka, Umeko Kawaharada, and Keiji Suzuki
日本原子力研究所高崎研究所材料開発部、群馬大学医学部泌尿器科、群馬大学医療短期大学部
Biomaterials, Vol. 10, Pages 16-22 (1989)
キーワード:制癌剤、シスプラチン、徐放性、針状製剤、コポリマー、ラット、腎臓、in vivo実験、壊死、
anticancer agent, cisplatin, controlled-release function, needle-type formulation, copolymer, rat, kidney, in vivo experiment, embolization
分類コード:010102, 010204, 010305

