作成: 2000/03/25 谷田貝 文夫
データ番号 :150018
放射線の種類によって細胞の照射後応答は違うのか
目的 :重イオン線照射に対する細胞応答の検討
研究実施機関名 :理化学研究所 細胞生理学研究室/ラジオアイソトープ技術室
応用分野 :放射線生物学、分子生物学
概要 :
ヒト培養細胞における重粒子線照射による致死、変異誘発、適応応答などの効果を、DNA修復やシグナル伝達系で重要な役割を果たしている蛋白の誘導や細胞周期の進行の様子などから検討している。X線照射に比べて癌抑制遺伝子p53産物の照射後誘導が時間的に遅れたり、停止がかかりにくくなる現象が鉄イオン(1000 KeV/mm)照射で観察された。炭素イオン(22 KeV/mm)照射ではX線と鉄イオンの場合の中間的なパターンを示した。重イオン照射によるDNA損傷の違いを示唆しているものと解釈される。
詳細説明 :
ヒト培養細胞における重粒子線照射による致死、変異誘発、Adaptation誘導などの効果を、DNA修復やシグナル伝達系で重要な役割を果たしている蛋白の誘導や細胞周期の進行の様子などから検討することを目的として、以下のような実験を行った。
理研リングサイクロトロンで加速した炭素、ネオン、鉄イオンなどをそのエネルギーを調節して、脾臓由来のリンパ芽球様細胞TK6およびWI-L2-NS(p53遺伝子のコドン237に変異をもつ細胞)に照射して致死、HPRT変異誘発、その後のX線照射効果の緩和(Adaptation)などを精力的に調べてきた。そこで、これらの得られた照射効果を基本的に理解するために,Western Blot法によるp53、p21などの蛋白の誘導やLaser Scan Cytometry法による細胞周期の分布を照射後の時間推的移も含めて蛋白レベルでの細胞の応答を調べることにした。今回の蛋白レベルでの検討には主に各イオンでの加速可能な最高エネルギーを用いた。
重イオンビームの特定エネルギー領域(それぞれのイオンで最大ビームエネルギー、いいかえれば、低LET領域)では、X線照射と類似した致死効果やHPRT突然変異誘発効果を示すが、それに対応してp53、p21などの蛋白の照射後誘導でもその類似性が認められた(図1)。
これら蛋白誘導の照射後時間推移を3 Gy照射したTK6細胞(p53遺伝子正常)についてより詳細に検討すると、炭素イオン(22 KeV/mm)照射はX線照射に比べて明確な差を示さないが、鉄イオン(1000 KeV/mm)照射は蛋白の誘導がピークに達するのに2倍位の時間(4時間)がかかる傾向を示した(図2)。また、5〜20 cGy程度の微量の炭素イオンを照射した細胞にその後本格的なX-線照射(Gyレベル)をすると、致死や変異誘発の緩和、いわゆるAdaptationとみなせる効果の可能性を否定できない(残念ながら統計的に有為な差はみられない)が、鉄イオンによる同じくらい低線量の予備照射による影響の可能性は低いものと判断された(図、表省略)。微量の重イオンの予備照射だけでもかなりのp53及びp21蛋白が誘導されるが、その後のX線照射によるこれら蛋白の誘導レベルにより上述のAdaptationの結果を説明できるかどうか現在検討している。
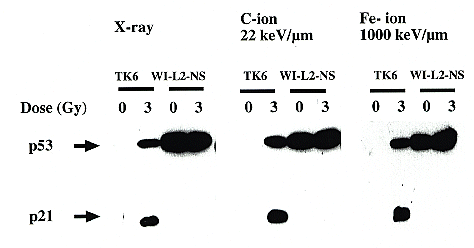
図1 重イオンビーム照射後のWI-L2-NS細胞とTK6細胞での蛋白誘導の比較(原論文1より引用)
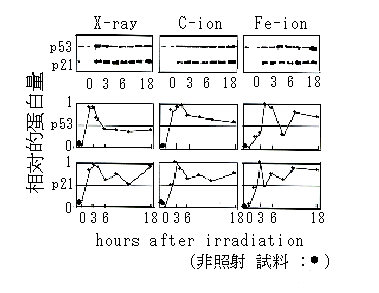
図2 重イオンビーム照射後のTK6細胞での蛋白誘導の時間的推移
いっぽう、3 G照射後の細胞周期分布の推移をみると、X線照射後6時間くらいでG2期の細胞が蓄積(G2停止)が起こるが、炭素イオン照射では照射後ゆっくりとG2期細胞の蓄積が起こりX線照射後6時間のレベルに達するには2倍くらいの12時間がかかった(表1)。驚いたことに、同様の鉄イオン照射では殆どG2期停止(蓄積)がかからず、照射後も非照射と同様の細胞周期分布が認められた。
表1 重イオンビーム照射後のTK6細胞での細胞周期分布の時間的推移
------------------------------------------------------------------------------
放射線 X線 炭素イオン(22keV/μm) 鉄イオン(1000keV/μm)
------------------------------------------------------------------------------
細胞周期 G1 S G2 G1 S G2 G1 S G2
非照射 46 37 18 48 36 16 42 42 16
照射直後 48 38 15 50 37 14 49 34 17
2時間後 37 40 23 42 37 21 42 34 24
3 34 44 22 40 35 25 41 35 25
4 31 39 31 35 29 31 44 34 22
6 24 20 55 32 30 36 45 25 30
9 23 16 60 29 25 44 43 30 28
12 21 11 58 28 18 53 41 26 33
18 17 6 69 22 10 62 43 28 24
------------------------------------------------------------------------------
これら蛋白レベルでの解析からも、重イオン照射によるDNA損傷の違いが示唆できるものと考えられる。
コメント :
今後は、個々の細胞での蛋白誘導を、とりわけ、微量放射線照射後に調べることが重要になるものと推測される。直接放射線の被ばくしない細胞への影響、いわゆるBystander Effectの研究や被ばく後長時間経過してからあらわれる遺伝的不安定性の問題の解決が急がれる。
原論文1 Data source 1:
Induction of p53 and p21 in human cells after heavy-ion irradiations.
Gordon A.J.E. , Fukunishi N., and Yatagai F.
The Institute of Physical and Chemical Research (RIKEN)
RIKEN Accelerator Progress Report, 32, 155 (1999).
原論文2 Data source 2:
Time course induction of p53 in human cell lines.
Gordon A.J.E. , Morimoto, S., Fukunishi N., and Yatagai F.
The Institute of Physical and Chemical Research (RIKEN)
RIKEN Accelerator Progress Report, 33, 131(2000).
原論文3 Data source 3:
Adaptive Response by Heavy-ion Irradiation in Human.Cultured Cell
Shigeko Morimoto, Alasdair Gordon, Nobuhisa Fukunishi, Toshihiro Kurobe, Fumio Hanaoka, and Fumio Yatagai
The Institute of Physical and Chemical Research (RIKEN)
RIKEN Accelerator Progress Report, 33, 142-143(2000).
参考資料1 Reference 1:
Effect of mutant p53 on the deletion profile of hprt mutations induced by heavy-ion irradiation.
Morimoto S., Gordon A.J.E. , Fukunishi N., Honma, M., Sofuni, T., Hanaoka F.,and Yatagai F.
The Institute of Physical and Chemical Research (RIKEN), National Institute of Health Sciences
Mutagenesis, submitted (2000)
参考資料2 Reference 2:
No G2 accumulation in the cell cycle in TK6 human lymphoblasoid cells after Fe-ion irradiation.
Gordon A.J.E. , Morimoto, S., Mizuno, T., Fukunishi N., Kurobe, T., Hanaoka, F., and Yatagai F.
The Institute of Physical and Chemical Research (RIKEN)
Int. J. Radiat. Biol., in preparation (2000)
参考資料3 Reference 3:
キーワード:重イオン照射, 線エネルギー付与率、ヒトリンパ芽球様細胞、蛋白誘導、ウエスタンブロット、細胞周期、がん抑制遺伝子、シグナル伝達、Heavy-ion, Linear Energy Transfer(LET), human lymphoblastoid cell, Protein Induction, Western Blot, Cell Cycle, Tumor Suppressor Gene, Signal Transducrion
分類コード:150102, 150302

