作成: 1999/01/06 谷田貝 文夫
データ番号 :150005
突然変異の特徴と放射線の線質
目的 :放射線により誘発される突然変異の解析手法の開発とその応用
研究実施機関名 :理化学研究所 細胞生理学研究室/ラジオアイソトープ技術室
応用分野 :放射線生物学、分子遺伝学
概要 :
原子炉の核燃料の製造や廃棄、医療での診断や治療など特殊な業務環境下での被曝をどのように軽減し、また、その危険性を推測するかは大変重要な課題になってきた。その推測には単に被曝線量だけでなく放射線の種類やエネルギーなどの因子も考慮する必要がある。ここではこれらの因子によって誘発される突然変異の特徴が異なることを最新のDNA解析技術の開発によって明らかにしたことについて述べる。
詳細説明 :
1.突然変異研究から放射線リスク評価へ
遺伝形質が親から子孫に誤って受け継がれることを突然変異といい、遺伝子の異常な変化が原因となる。その変化には遺伝子DNA塩基配列中の特定のわずか1塩基が別の塩基に置き換わる(塩基置換)。1,2の塩基が付加されたり欠失して次々にコードするアミノ酸が変わってしまう(フレームシフト)。そして、塩基配列が大きく欠失(デリーション)したり大きく変化(リアレンジメント)したりすることなどがある。今までに集積された突然変異のデータベースから、変異に結びつくDNA損傷もかなりの程度推測することができる。しかしながら、放射線によるDNA損傷は化学薬剤などの場合と異なり、多種多彩なのでその推測はかなり難しい。ここでは、近年注目を浴びている「特殊な業務環境下での被曝」で問題になりうる重粒子イオン線(α線なども含めて)について取り上げてみたい。重粒子イオン線照射による突然変異の誘発の特異性に関する研究からの放射線リスク評価へのアプローチである。
2.X線、γ線などの電離放射線と重粒子ビームの違い
物理的に考えると放射線を浴びる物質へのエネルギー付与が異なる、すなわちX線やγ線では物質全体に均一に電離が起こるが重粒子ビームではその飛跡に沿って電離が起こる。重粒子ビーム照射の場合は、その粒子のエネルギーによって上述の電離の頻度、つまりエネルギー付与が異なるので線エネルギー付与率(LET)という単位がよく用いられる。そこで、このLETの違いによって放射線の相対的生物効果(RBE)がどのように変化するかを調べる研究に関心が寄せられている。私たちがここ数年で集中して研究を進めているヒト胎児初代培養(HE)細胞に対して重イオンビームを照射した場合について、その致死効果のRBEのLET依存性を調べた結果を簡単に紹介する。ネオンイオンビーム照射ではいわゆるRBEのピークは幅が広くなって、炭素イオン照射の場合のLET120keV/mm付近での鋭いピークを与える場合とは少し異なったプロファイルを示した。
3.重粒子イオン線の止まり際での突然変異誘発
LETが先程のRBEのピークを与える値よりも高い領域でのビームの止まり際、すなわち、ビームは細胞を通過するとすぐに止まってしまうようなLET230keV/μmでのHE細胞のヒポキサンチンリボシル転移酵素(hprt)遺伝子座における突然変異を調べてみた。この結果、点突然変異(塩基置換やフレームシフト)が大多数であったので、ヒトリンパ芽球用細胞(TK6)を利用して、この現象の普遍性について調べてみることにした。この際に、炭素イオンは250keV/μm、ネオンイオンは310keV/μmを利用して、より詳細に調べることにした。表1aに示すように、このような照射条件下でもHPRT変異は自然突然変異(非照射)に比べて明らかに高い誘発率を示した。HPRT遺伝子座のゲノムDNAに対する多重PCR(Polymerase Chain Reaction)法(図1)により得られたHPRT変異体の変異の詳細解析の結果から、炭素イオンとネオンイオンビーム照射ではその特徴がかなり異なることが明確になった(表1b)。
表1 重イオンビーム照射後のHPRT突然変異の誘発(a)と多重PCR法による分類(b)(原論文2より引用)
a)
--------------------------------------------
Heavy Ion - C Ne
--------------------------------------------
LET(keV/μm) - 250 310
--------------------------------------------
Dose(Gy) 0 3.0 3.0
--------------------------------------------
Surviving Fraction 1.0 0.23 0.20
--------------------------------------------
Mutation Frequency(x10-6) 0.6 2.7 4.4
--------------------------------------------
b)
------------------------------------------------
PCR Amplification Number of mutant clones
Patten ---------------------------
C-ion Ne-ion
(250keV/μm) (310keV/μm)
------------------------------------------------
Normal 10a 3
Exon loss 9 17
(Complex loss)b (3) (3)
Total 19 20
------------------------------------------------
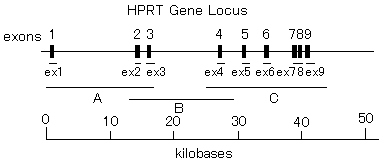
図1 ヒトHPRT遺伝子座における突然変異の多重PCR法およびLong PCR法による解析の概略(原論文2より引用)
炭素イオンの場合はHE細胞と同様に塩基置換型変異(多重PCRパターンは正常)が多く、いっぽう、ネオンイオンビーム照射ではHPRT遺伝子のエクソン領域によっては増幅されないパターン、いわゆる欠失型変異が多数であった。図1のネオンイオンでの致死効果のRBEピークがLETに対して幅広くなった結果を反映しているように考えられる。つまり、HE細胞に対して、RBEピークを与える領域で炭素イオンビームを照射して欠失変異が多く観察された結果とつじつまが合っている。
コメント :
「特殊な業務環境下での被曝」の可能性について上述したが、高自然放射線バックグラウンドで又は原子力発電所の事故等によって同様な環境で生活する人々や、さらには航空機や宇宙飛行関係者などに対してもその危険性を考慮しなければならない。ここで述べた、放射線によって誘発される突然変異の特徴からこれらの問題にアプローチすることは大変意義深いものと考えられる。放射線等によるDNA損傷、とりわけDNA2重鎖切断はその傷が情報(シグナル)伝達のきっかけとなる。そのきっかけで細胞内の蛋白のりん酸化やたん白とたん白の相互作用を通して、細胞周期(チェックポイント)のコントロールとも関連して、DNA修復を促進したり、アポトーシスにより細胞は致死に向かうが組織としてはその命を救う。
今後は、このような修復系に関与する突然変異、あるいは、傷そのものをバイパスしてしまうと考えられる。いわゆる、DNA translation synthesisでの突然変異などについて、ここで述べた突然変異の特異性とどのように結びつくのかについても研究を進めていく必要がある。
原論文1 Data source 1:
LET dependence of cell death and chromatin-break induction in normal human cells irradiated by neon-ion beams
Suzuki M., Kase Y., Kanai T., Yatagai F., and Watanabe M.
National Institute of Radiological Sciences, Nagasaki University, The Institute of Physical and Chemical Research
Int. J. Radiat. Biol., 72, 497-503 (1997).
原論文2 Data source 2:
Complex HPRT deletion events are recovered after exposure of human lymphoblastoid cells to high-LET carbon and neon ion beams
Kagawa Y., Shimazu T., Gordon A.J.E. , Fukunishi N., Inabe N., Suzuki M., Hirano M., Kato T., Watanabe M., and Hanaoka F. and Yatagai F.
)National Institute of Radiological Sciences, Nagasaki University, The Institute of Physical and Chemical Research, Osaka University, and Yokohama City University
Mutagenesis, 14, 199-205 (1999).
参考資料1 Reference 1:
Analysis of Mutations in the Human HPRT Gene Induced by Accelerated Heavy-Ion Irradiation
Kagawa Y, Yatagai F, Suzuki M, Kase Y, Kobayashi A, Hirano M, Kato T, Watanabe M, and Hanaoka F.
The Institute of Physical and Chemical Research, Toray Research Center Inc., National Institute of Radiological Sciences, Osaka University, and Nagasaki University
J. Radiat. Res., 36, 185-195 (1995)
参考資料2 Reference 2:
LET Deoendence of cell death, mutataion induction and chromatin damage in human cells irradiated with accelerated carbon ions
Suzuki M, Watanabe M, Kanai T, Kase Y, Yatagai F, Kato T, and Matubara S.
National Institute of Radiological Sciences, Nagasaki University, The Institute of Physical and Chemical Research, Osaka University, and Yokohama City University
Adv. Space. Res., 18, 127-136 (1996)
キーワード:重イオンビーム照射, 線エネルギー付与率、ヒト胎児初代培養細胞、ヒポキサンチンリボシル転移酵素変異、多重PCR、DNA 塩基配列決定、
Heavy-ion Beam Irradiation, Linear Energy Transfer(LET), human embryo cell, HPRT Mutation, Multiplex PCR, DNA Sequencing
分類コード:150101, 150302
